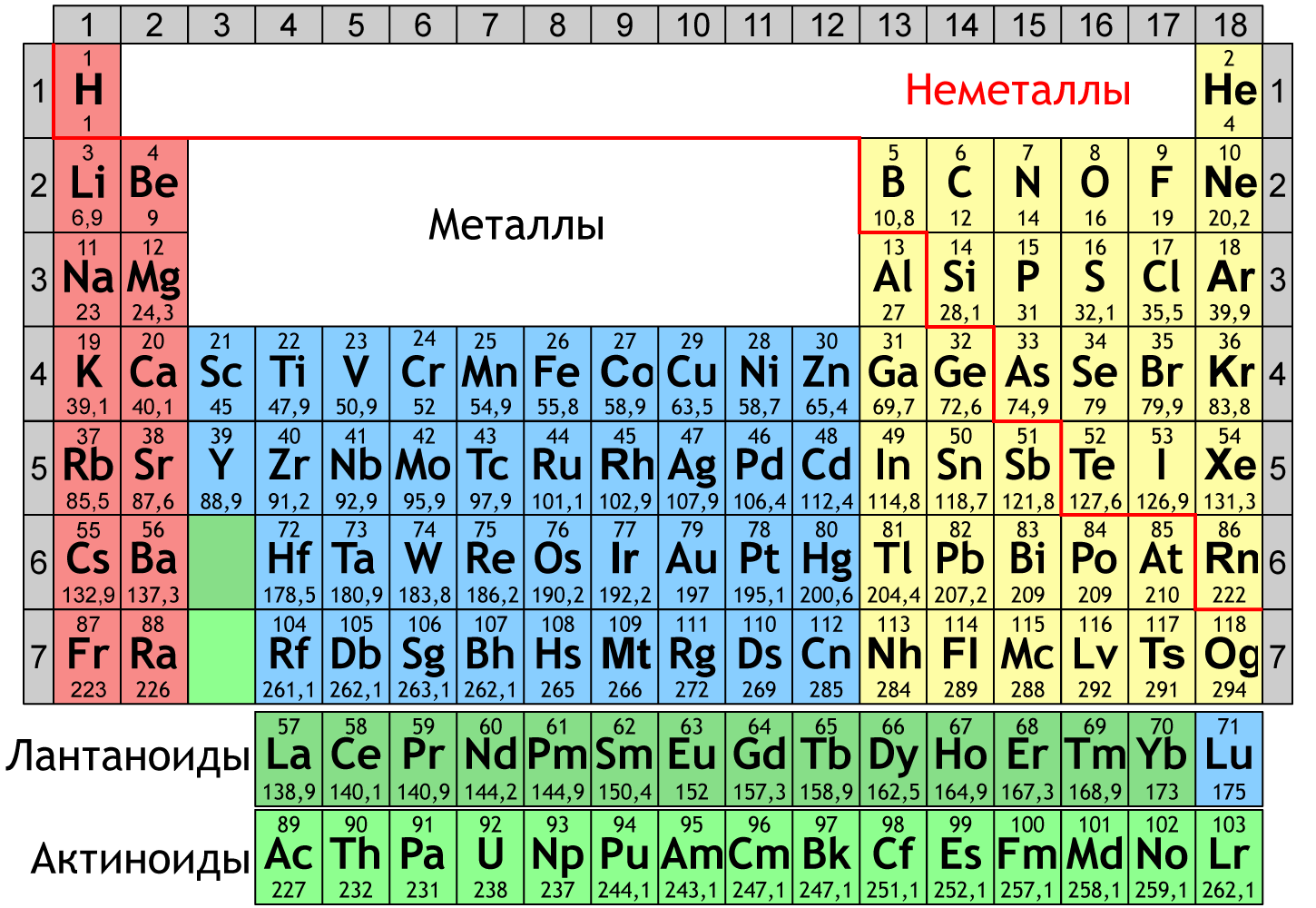
В Периодической системе химических элементов металлы расположены ниже диагонали В–At в главных подгруппах, а также во всех побочных подгруппах.
На внешнем энергетическом уровне атомов металлов находится 1–3 электрона. Исключение составляют Ge, Sn, Pb (4e–), Sb и Bi (5e–) и Po (6e–).
Все металлы – восстановители. В химических реакциях они легко отдают внешние электроны. Образуются катионы, внешняя оболочка которых подобна оболочке инертных газов. Это обеспечивает им устойчивость.
Для металлов характерна низкая электроотрицательность.
С увеличением заряда ядра атома металла:
в периоде: электроотрицательность увеличивается, а металлические свойства уменьшаются;
в группе: электроотрицательность уменьшается, а металлические свойства усиливаются.
Для металлов характерна металлическая кристаллическая решётка, которая определяет физические свойства металлов: твёрдость, блеск, ковкость, тепло- и электропроводность.