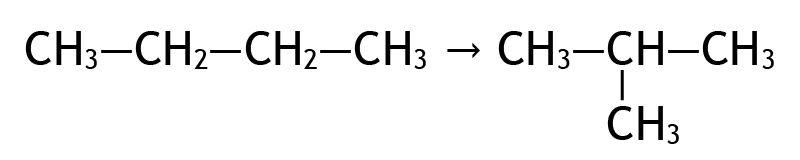- Для алканов характерны реакции замещения (механизм свободно-радикальный).
СН4 + Cl2 → CH3Cl + HCl; CH3Cl + Cl2 → CH2Cl2 + HCl;
CH2Cl2 + Cl2 → CHCl3 + HCl; CHCl3 + Cl2 → CCl4 + HCl.
- При освещении смеси метана с хлором реакция идёт со взрывом.
- Все предельные углеводороды горят на воздухе с выделением тепла:
СН4 + 2О2 → СО2 + 2Н2О + 890 кДж.
- Смесь метана с воздухом (1:10) или кислородом (1:2) взрывоопасна.
- При нагревании выше 1000 оС без доступа воздуха алканы разлагаются:
СН4 → С + 2Н2.
- При нагревании до температуры 1500 оС без доступа воздуха образуется ацетилен:
2СН4 → HС≡СН + 3Н2.
- При нагревании этана до 1500 оС без доступа воздуха в присутствии никелевого катализатора образуется этилен:
CH3–CH3 → СН2=СН2 + Н2.
- В присутствии катализатора AlCl3 нормальные алканы подвергаются изомеризации: